리보솜
본 서비스가 제공하는 내용 및 자료가 사실임을 보증하지 않습니다. 시스템은 언제나 실수를 할 수 있습니다. 중요한 의사결정 및 법리적 해석, 금전적 의사결정에 사용하지 마십시오.
리보솜(ribosome)은 모든 살아있는 세포에 존재하며 단백질 합성을 담당하는 세포소기관이다. 리보솜 RNA(rRNA)와 단백질로 구성되어 있으며, 크기가 서로 다른 두 개의 소단위체가 결합하여 기능을 수행한다. 유전 정보가 담긴 전령 RNA(mRNA)의 코돈을 읽어 아미노산을 순서대로 배열함으로써 폴리펩타이드 사슬을 형성하는 번역 과정을 주도한다.
개요 및 역사
리보솜은 1950년대 중반 루마니아의 생물학자 조지 에밀 펄레이드(George Emil Palade)가 전자현미경을 통해 최초로 관찰하였다. 펄레이드는 이 공로로 1974년 노벨 생리학·의학상을 수상하였다. '리보솜'이라는 명칭은 1958년 리처드 B. 로버츠가 리보핵산(ribonucleic acid)의 'ribo'와 몸을 뜻하는 그리스어 'soma'에서 유래한 접미사 '-some'을 결합하여 제안하였다. 이후 리보솜의 구조와 기능을 밝힌 공로로 아다 요나트, 벤카트라만 라마크리슈난, 토머스 A. 스타이츠가 2009년 노벨 화학상을 공동 수상하였다.
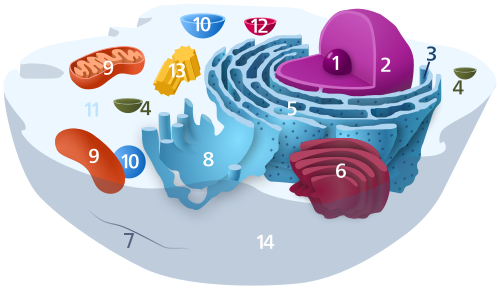
구조와 성분
리보솜은 별도의 세포막이 없는 입자 형태의 기관이다. 지름은 약 20nm이며, 크게 대단위체와 소단위체로 나뉜다. 구성 성분은 리보솜 RNA(rRNA)가 약 6065%, 단백질이 약 3540%를 차지한다. 진핵생물의 경우 세포질에서 생성된 단백질이 핵으로 들어가 rRNA와 결합하여 소단위체들을 형성한 뒤, 다시 세포질로 나와 최종적인 리보솜 구조를 완성한다.
단백질 합성 과정
리보솜은 mRNA의 유전 암호를 해독하여 단백질을 만드는 번역(translation) 과정을 수행한다. 과정은 크게 초기화, 연장, 종결 단계로 구분된다.
- A 자리(Aminoacyl site): 새로운 아미노산을 가진 tRNA가 들어오는 자리이다.
- P 자리(Peptidyl site): 아미노산 사슬(폴리펩타이드)이 신장되는 자리이다.
- E 자리(Exit site): 아미노산을 전달한 tRNA가 리보솜을 떠나는 자리이다.
소단위체가 mRNA와 결합하고 개시 코돈을 확인하면 대단위체가 결합하여 합성을 시작한다. 운반 RNA(tRNA)가 아미노산을 순서대로 가져오면 리보솜이 이를 연결하여 단백질을 형성한다.

분류 및 위치
리보솜은 세포 내 존재하는 위치와 상태에 따라 두 가지로 분류된다.
- 자유 리보솜(Free ribosome): 세포질에 자유롭게 떠다니며 주로 세포 내부에서 사용되는 단백질을 합성한다.
- 부착 리보솜: 거친면 소포체(ER)의 표면에 붙어 있으며, 주로 세포 밖으로 분비되거나 막에 삽입될 단백질을 합성한다.